Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (46): 8122-8127.doi: 10.3969/j.issn.2095-4344.2013.46.023
Previous Articles Next Articles
Tissue-engineered cartilage repair for sports-induced articular cartilage injury
Zhang Lu-yao
- Department of Physical Education, Huaiyin Institute of Technology, Huaian 223003, Jiangsu Province, China
-
Online:2013-11-12Published:2013-11-30 -
About author:Zhang Lu-yao★, Department of Physical Education, Huaiyin Institute of Technology, Huaian 223003, Jiangsu Province, China
CLC Number:
Cite this article
Zhang Lu-yao. Tissue-engineered cartilage repair for sports-induced articular cartilage injury[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(46): 8122-8127.
share this article
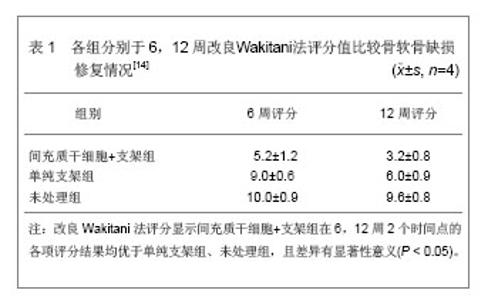
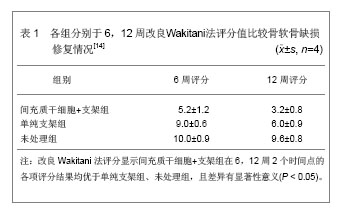
2.1 构建组织工程化软骨的要素 2.1.1 种子细胞的来源 种子细胞的选择是组织工程化软骨研究的重点之一。如何选择合适的细胞以及如何改良种子细胞是构建组织工程化软骨的关键。理想的组织工程化软骨的种子细胞应该具备以下几个特 点[18]:①取材方便,来源广泛且对机体损伤小。②增殖能力强,体外易于培养和扩增。③能适应材料和受区环境,对于相应的支架材料,黏附能力强。④能在受区完全替代缺失细胞的功能,适应不同应力条件。 自体软骨细胞:软骨细胞的主要功能是维持软骨基质成分的稳定。软骨细胞在体外和体内移植研究中均证实可靠的软骨形成效果。自体软骨细胞分离和培养简单,同源性好,无免疫排斥问题,但其在人体来源有限,限制了其临床应用。夏万尧等[19]探讨了组织工程化软骨组织形成的最佳细胞浓度和最佳形成时间,结果发现形成软骨组织最适细胞浓度为50× 109 L-1,最佳形成时间是第6周。然而从少量的自体软骨组织经过体外分离培养获得50×109 L-1这么大量数目的种子细胞,是难以实现的。因此,以自体的软骨细胞作为种子细胞,其来源有限[20]。同时获取自体软骨细胞需要有创操作,易引起感染等相关并发症的发生。由此可见,重要的是这些细胞必须容易获得,而且不会对供区产生较大的影响,因为此类操作导致了额外的损伤,并且没有从力学上改变组织特性[21]。 同种异体软骨细胞:同种异体来源的软骨细胞具有来源广泛、一次可获取大量细胞、取材容易等优点[22]。对于同种异体软骨细胞的生物学特性和相关免疫反应问题的进一步研究,将为建立构建组织工程化软骨的种子细胞库奠定基础。Vunjak-Novakovic等[23]通过研究已经得到证明,同种异体软骨细胞可在受体内长期生长并保持分泌基质的功能。与自体软骨细胞相比,应用前景比较广阔。目前,如何在体外调控种子细胞的生长和增殖使其分泌正常的基质,依然是研究的重点,同时建立大规模的种子细胞培养系统也是必要的[24]。 2.1.2 支架材料的选择 Rahman等[25]比较了几种生物材料本身对软骨细胞增殖的作用,发现刺激效应依次为聚乙交酯﹥聚乳酸﹥聚乳酸乙醇酸共聚物﹥左旋聚乳酸,表明构建组织工程化软骨时,选择支架的生物材料也相当重要。理想的软骨组织工程支架应具有良好的生物相容性、良好的表面活性、生物可降解性、足够的孔隙结构、促进细胞黏附于增殖、具备承载生长因子的能力、可塑性和一定的机械强度[26]。现今有多种支架材料被用于组织工程化软骨的构建,按其来源不同大体可分为天然和人工合成的两种[27]。 天然生物材料:天然生物支架材料来源于生物体本身,主要包括胶原、明胶、纤维蛋白、壳聚糖、琼脂、糖胺多糖、藻酸盐、蚕丝蛋白等[28]。天然支架的优势在于材料的组织相容性较好,毒性较小,易被吸收降解,且降解的产物易被人体所吸收,而且不产生炎症反应等。但天然材料因其来源的不同,结构与性能存在批次间的差异,因此,就需要统一材料的质量标准,且因其来自于天然生物体,如果处理不当尚有传播疾病的危险。Wambach等[29]从狗甲状软骨上获得的软骨细胞种植到牛Ⅰ型胶原纤维上体外培养,以Ⅰ型胶原为支架培养软骨细胞,结果发现细胞存活并表达其自身表型,产生细胞外基质,取得较为满意的结果。 人工合成高分子材料:人工合成高分子材料的微结构、机械性能以及材料的降解时间等都可以预先设计和调控[30]。包括聚乳酸、聚羟基乙酸、乳酸和乙醇酸共聚物等脂肪族聚酯。目前运用较广泛的聚乙醇酸、聚乳酸由于具有良好的生物相容性已被用于组织工程支架材料[31]。而且由于材料的可吸收性,使其在软骨细胞生长、软骨基质分泌的过程中逐渐降解,为新生软骨组织所替代。但作为组织工程化软骨的支架材料,人工合成高分子材料最大缺点是材料表面缺乏细胞可以识别的位点,不具备生物活性,而且材料的降解产物可能存在一定的毒性作用限制了它的应用。1995年,Baldwin等[32]将关节软骨细胞种植于聚乳酸支架上,移植至实验动物的软骨缺损处,移植6周后,动物软骨缺损处生长出新生的软骨组织,体外培养结果证明软骨细胞在生物支架中具有较高的细胞活性。李旭升等[33]以快速成形的聚乙丙交酯三维支架接种骨髓基质细胞,可见,细胞在支架上大量扩增,成功构建出软骨样组织。Uematsu等[34]在同种细胞移植中以聚乙丙交酯为生物支架,将间充质干细胞移植于有大片骨缺损的兔膝关节内,可以成功的诱导出软骨组织。 2.2 影响组织工程化软骨构建的因素 在组织工程化软骨构建中,影响细胞生长、增殖及分化的因素很多,其中生长因子、力学因素、氧浓度、应力、微重力 等[35]。目前所面临的挑战是确定影响组织工程化软骨构建的因素,以便用于逐渐复杂化的动物模型,并最终服务于临床。 2.2.1 种子细胞浓度 种子细胞的体外培养和增殖是组织工程化软骨研究的主要内容,种子细胞的数量会直接影响到组织工程化软骨的质量和体积。要得到组织工程化软骨,高浓度的细胞接种浓度是必需的。张瑛等[36]探讨了兔组织工程化软骨形成的合适细胞浓度。分离培养兔关节软骨细胞,在体外扩增后以1,2,4,6,8,10×1010 L-1 6种不同的细胞浓度种植到聚乳酸聚乙醇酸的生物支架上,在体外培养软骨细胞支架复合物,4周终止培养,进行苏木精-伊红、Masson组织学染色、Ⅱ型胶原免疫组织化学染色,结果见表1。 2.2.2 生物力学的影响 关节软骨所处的特殊环境,使研究者们注意到模拟关节内生物力学环境对研究软骨组织形成的重要性。近年来,随着组织工程技术的快速发展,开展体外构建组织工程化软骨的研究越来越被人们所重视。为在体外培养出具有更佳生物学活性和力学性能的组织工程化软骨,应考虑到尽量在体外模拟软骨细胞在体内的生长环境,需要给予软骨细胞一定的力学刺激。毛艳等[37]在压应变作用下构建组织工程化软骨。以大鼠的骨髓间充质干细胞为种子细胞,以壳聚糖海绵为支架材料,利用压应变加载装置对细胞-壳聚糖海绵支架材料的复合物进行体外动态加载研究,构建的组织工程化软骨经过体内移植后,分泌软骨基质Ⅱ型胶原及酸性糖胺多糖,其弹性模量较植入前有显著的增强,在压应变的作用下,细胞复合壳聚糖支架材料可以形成初级的组织工程化软骨。Martin等[38]对人软骨细胞进行低氧张力的培养研究,同时也证实了低氧张力对软骨细胞的增殖潜能是有利的,而过高的氧浓度会对细胞的DNA产生损伤。 2.2.3 生长因子 生长因子对软骨细胞生长、增殖起着重要作用,作为关节软骨有丝分裂原,生长因子促进软骨细胞增殖,同时并使增殖的细胞稳定的向成熟软骨细胞分化。这些因子包括形态发生蛋白、转化生长因子、碱性成纤维细胞生长因子、胰岛素样生长因子、表皮生长因子等[39]。目前已知最强的促细胞生长因子是碱性成纤维细胞生长因子。其他生长因子,如肝细胞生长因子、血小板衍生生长因子等对关节软骨的形成也具有调控作用。 Mohan等[40]研究发现软骨内含有许多细胞因子及其受体,并且表明这些细胞因子通过自分泌和旁分泌这两种分泌基本方式来调节软骨的生成。此外,因中医药类似生长因子的作用在软骨组织工程中逐渐受到重视,对其深入系统的研究将是组织工程化软骨进一步完善的又一突破点[41-42]。不同的因子互相影响,彼此想成复杂的网络关系,对种子细胞造成不同层次的影响。 2.2.4 其他影响因素 在适当的时间范围内施以适当的压力可以促进单层培养的软骨细胞增殖和基质的分泌,而超过一定的限度则会产生抑制的作用。Falsafi等[43]研究发现软骨细胞在微重力状态下能迅速增殖,在短时间内分裂达较高的数量级别,克服了常规的培养时间长、增殖慢的缺点。气体环境对软骨细胞培养的影响早就被人们所认识,骨髓间充质干细胞向软骨细胞诱导时也不例外。O'Driscoll等[44]研究发现氧浓度过高、过低都不利于软骨细胞生长、繁殖及代谢。 2.3 组织工程化软骨的应用 组织工程化软骨修复软骨缺损突破了传统关节软骨的修复理念,为关节软骨获得完全性组织修复重建和功能恢复提供了新途径。可以说组织工程化软骨是一种可行的修复关节软骨缺损的有效方法。众多学者通过各种实验尝试用组织工程化软骨来修复关节缺损,并获得较为满意的效果。Kim等[45]用可降解多聚材料聚乳酸乙醇酸共聚物,按照所需制成各种形状,再将新鲜的软骨细胞植入支架材料上,体外培养1周后移植入体内,同样形成透明软骨组织。曹峻岭等[46]使用两种不同来源的种子细胞和两种不同的复合骨基质明胶构建组织工程化软骨,并且进行了软骨损伤机理和软骨缺损修复的实验研究。不仅验证了构建组织工程化软骨的可行性和有效性,还为其在实验室和临床上的应用提供了科学依据。 组织工程化软骨在修复软骨缺损中有三大优点:①软骨细胞可在体外培养及增殖,且只需少量的自体软骨细胞就可获得足够移植用的细胞数量。②可根据需要设计、制作各种形状、大小的三维支架。③体外构建的软骨组织修复关节缺损时可以避免发生免疫排斥反应。宋红星等[47]结合体外实验结果,认为松质骨骨基质明胶是一种较好的、可以用于修复关节软骨缺损的软骨细胞支架材料,在软骨缺损处使用胰蛋白酶还可以促进修复组织与宿主缺损周围组织的愈合。Kimura等[48]结合关节镜技术,用可注射的液体聚合物与软骨细胞混合培养后移植于皮下,最终形成与正常软骨组织结构、机械性能都十分相似的软骨组织。这些实验表明细胞-支架复合物这种组织工程化软骨,治疗运动性关节软骨损伤是可行的。同时值得注意的是,实验动物模型不具备临床意义,仅为临床治疗提供基本的原则和引导,动物实验的局限性已经广泛受到重视。兔、狗、羊的关节软骨厚度仅相当于人关节软骨厚度的一部分,任何修复人关节软骨的研究必须克服这一问题。 "
| [1]刘忆冰.软骨修复材料对运动性膝关节软骨损伤的修复[J].中国组织工程研究与临床康复,2009,13(12):2337-2340. [2]闫领先.腕关节软骨损伤的生物材料干预[J].中国组织工程研究与临床康复,2010,14(134):6445-6448. [3]Vo N, Niedernhofer LJ, Nasto LA, et al.An overview of underlying causes and animal models for the study of age-related degenerative disorders of the spine and synovial joints.J Orthop Res.2013;31(6):831-837. [4]Capeci CM, Turchiano M, Strauss EJ, et al.Osteochondral allografts: applications in treating articular cartilage defects in the knee.Bull Hosp Jt Dis (2013).2013;71(1):60-67. [5]Clouet J, Vinatier C, Merceron C, et al.From osteoarthritis treatments to future regenerative therapies for cartilage.Drug Discov Today.2009;14(19-20):913-925. [6]张仲文,侯世科,杨造成,等.基质诱导的自体软骨细胞移植术修复膝关节软骨缺损10例术后2年的随访[J].中华关节外科杂志(电子版),2010,4(6):17-21. [7]张永涛,金丹.组织工程骨软骨复合体构建的研究进展[J].中国修复重建外科杂志,2011,25(9):1120-1124. [8]王慎东.自体及异体骨软骨移植与骨缺损修复[J].中国组织工程研究与临床康复,2008,12(40):7905-7908. [9]Komárek J, Vališ P, Repko M, et al.Treatment of deep cartilage defects of the knee with autologous chondrocyte transplantation: long-term results.Acta Chir Orthop Traumatol Cech. 2010;77(4):291-295. [10]Boyan BD, Sylvia VL, McKinney N, et al.Membrane actions of vitamin D metabolites 1alpha,25(OH)2D3 and 24R,25(OH)2D3 are retained in growth plate cartilage cells from vitamin D receptor knockout mice.J Cell Biochem. 2003;90(6):1207-1223. [11]Lim HC, Bae JH, Song SH, et al.Current treatments of isolated articular cartilage lesions of the knee achieve similar outcomes. Clin Orthop Relat Res. 2012;470(8): 2261-2267. [12]Green WT Jr.Articular cartilage repair. Behavior of rabbit chondrocytes during tissue culture and subsequent allografting.Clin Orthop Relat Res.1977;(124):237-250. [13]Kato Y,Iwamoto M,Koike T,et al.Terminal differentiation and calcification in rabbit chondrocyte cultures grown in centrifuge tubes: regulation by transforming growth factor beta and serum factors.Proc Natl Acad Sci U S A.1988;85(24):9552-9556. [14]Wakitani S,Kimura T,Hirooka A,et al.Repair of rabbit articular surfaces with allograft chondrocytes embedded in collagen gel.J Bone Joint Surg Br.1989;71(1):74-80. [15]颜炜群,佟明华,宇莉,等.培养软骨细胞再形成生长板软骨组织的研究[J].实验生物学报,1994,2(27):193-196. [16]中国知网.中国学术期刊总库[DB/OL].2013-8-15.https://www.cnki.net [17]SCI数据库.Web of Sciencevia ISI Web of Knowledge[DB/OL].2013-8-15.http://ip-science.thomsonreuters.com/mjl [18]周广东,崔磊,刘伟,等.软骨组织工程的历史、现状与未来[J].整形再造外科杂志,2004,1(1):52-56. [19]夏万尧,曹谊林,商庆新,等.组织工程化软骨组织形成的最佳细胞浓度和最佳形成时间的实验研究[J].中国修复重建外科杂志,1999,13(4):442-446. [20]Kelly TA, Roach BL, Weidner ZD, et al.Tissue-engineered articular cartilage exhibits tension-compression nonlinearity reminiscent of the native cartilage.J Biomech. 2013;46(11):1784-1791. [21]Gardner OF, Archer CW, Alini M, et al.Chondrogenesis of mesenchymal stem cells for cartilage tissue engineering.Histol Histopathol.2013;28(1):23-42. [22]Schwarz S, Koerber L, Elsaesser AF, et al.Decellularized cartilage matrix as a novel biomatrix for cartilage tissue-engineering applications.Tissue Eng Part A. 2012;18(21-22):2195-2209. [23]Vunjak-Novakovic G,Obradovic B,Martin I,et al.Dynamic cell seeding of polymer scaffolds for cartilage tissue engineering.Biotechnol Prog.1998;14(2):193-202. [24]Cheng H, Byrska-Bishop M, Zhang CT, et al.Stem cell membrane engineering for cell rolling using peptide conjugation and tuning of cell-selectin interaction kinetics.Biomaterials. 2012;33(20):5004-5012. [25]Rahman MS,Tsuchiya T.Enhancement of chondrogenic differentiation of human articular chondrocytes by biodegradable polymers.sue Eng.2001;7(6):781-790. [26]刘清宇,王富友,杨柳.关节软骨组织工程支架的研究进展[J].中国修复重建外科杂志,2012,26(10):1247-1250. [27]贵浩然,李澎,张卫国.制备软骨组织工程支架的材料和方法[J].中国组织工程研究,2013,17(3):509-516. [28]梁卫东,王宏伟,王志强.不同骨组织工程支架材料的生物安全性及性能[J].中国组织工程研究与临床康复,2010,14(34):6385-6388. [29]Wambach BA,Cheung H,Josephson GD.Cartilage tissue engineering using thyroid chondrocytes on a type I collagen matrix.Laryngoscope.2000;110(12):2008-2011. [30]杨立群,杨丹,孟舒,等.生物降解性合成高分子材料作为药物缓释载体的研究进展[J].当代医学,2009,15(33):16-18. [31]Xu H, Han D, Dong JS, et al.Rapid prototyped PGA/PLA scaffolds in the reconstruction of mandibular condyle bone defects.Int J Med Robot.2010;6(1):66-72. [32]Baldwin SP,Krewson CE,Saltzman WM.PC12 cell aggregation and neurite growth in gels of collagen, laminin and fibronectin.Int J Dev Neurosci.1996;14(3):351-364. [33]李旭升.组织工程骨软骨复合物修复兔关节骨软骨缺损及其相关研究[D].陕西:第四军医大学,2005:1-106. [34]Uematsu K,Hattori K,Ishimoto Y,et al.rtilage regeneration using mesenchymal stem cells and a three-dimensional poly-lactic-glycolic acid (PLGA) scaffold.Biomaterials.2005;26(20):4273-4279. [35]李元城,张卫国,秦建华,等.微流控芯片上胰岛素样生长因子1和碱性成纤维细胞生长因子对兔关节软骨细胞增殖的影响[J].解放军医学杂志,2013,38(6):476-480. [36]张瑛,范卫民,陈哲峰.组织工程化软骨形成的细胞浓度选择[J].江苏医药,2005,31(10):762-764. [37]毛艳,张西正,李瑞欣,等.压应变作用下组织工程软骨的构建[J].中国生物医学工程学报,2008,27(2):297-302. [38]Martin JA,Klingelhutz AJ,Moussavi-Harami F,et al.Effects of oxidative damage and telomerase activity on human articular cartilage chondrocyte senescence.J Gerontol A Biol Sci Med Sci.2004;59(4):324-337. [39]Place ES, Nair R, Chia HN, et al.Latent TGF-β hydrogels for cartilage tissue engineering.Adv Healthc Mater. 2012;1(4):480-484. [40]Mohan S,Baylink DJ.growth factors.Clin Orthop Relat Res.1991;(263):30-48. [41]郑晓辉,屠永刚,夏雄智,等.肾行气活血法在骨髓基质干细胞诱导软骨细胞修复兔关节软骨缺损中的作用[J].中国矫形外科杂志,2008,16(16):1227-1230. [42]张春霞,修忠标.鹿茸多肽对兔骨髓间充质干细胞移植修复关节软骨缺损的影响[J].福建中医学院学报,2007,17(4):16-19. [43]Falsafi S,Koch RJ.Growth of tissue-engineered human nasoseptal cartilage in simulated microgravity.Arch Otolaryngol Head Neck Surg.2000;126(6):759-765. [44]O'Driscoll SW,Fitzsimmons JS,Role of oxygen tension during cartilage formation by periosteum.J Orthop Res.1997;15(5):682-687. [45]Kim WS,Vacanti JP,Cima L,et al.Cartilage engineered in predetermined shapes employing cell transplantation on synthetic biodegradable polymers.Plast Reconstr Surg.1994;94(2):233-237. [46]曹峻岭,付强.组织工程化软骨的构建及应用[J].西安交通大学学报(医学版),2008,29(2):121-127. [47]宋红星,沈惠良,王民,等.松质骨骨基质明胶负载软骨细胞移植修复兔膝关节软骨缺损[J].中华风湿病学杂志,2003,7(11):678-680. [48]Kimura T,Yasui N,Ohsawa S,et al.Chondrocytes embedded in collagen gels maintain cartilage phenotype during long-term cultures.Clin Orthop Relat Res.1984;(186):231-239. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [3] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [4] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [5] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [6] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [7] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [8] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [9] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [10] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [11] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [12] | Guan Jian, Jia Yanfei, Zhang Baoxin , Zhao Guozhong. Application of 4D bioprinting in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 446-455. |
| [13] | Liu Jiali, Suo Hairui, Yang Han, Wang Ling, Xu Mingen. Influence of lay-down angles on mechanical properties of three-dimensional printed polycaprolactone scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2612-2617. |
| [14] | Huang Bo, Chen Mingxue, Peng Liqing, Luo Xujiang, Li Huo, Wang Hao, Tian Qinyu, Lu Xiaobo, Liu Shuyun, Guo Quanyi . Fabrication and biocompatibility of injectable gelatin-methacryloyl/cartilage-derived matrix particles composite hydrogel scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2600-2606. |
| [15] | Fang Xiaoyang, Tang Tian, Wang Nan, Qian Yuzhang, Xie Lin. Repair and regenerative therapies of the annulus fibrosus [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(10): 1582-1587. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||